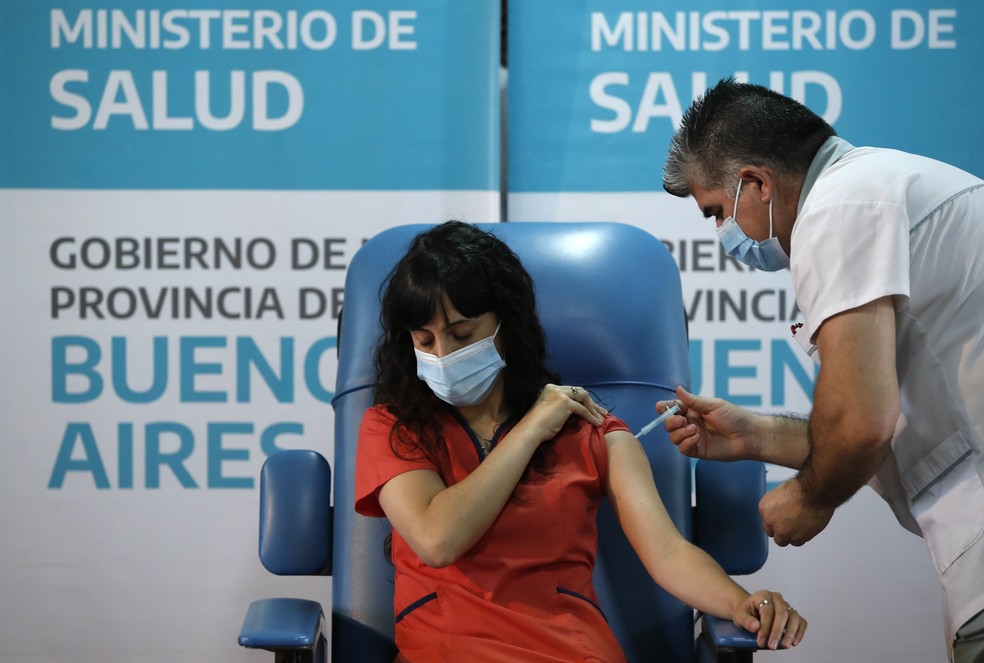
O enfermeiro Gustavo Rodriguez aplica a vacina Sputnik V contra a Covid-19 na médica Estefania Zevrnja em hospital em Avellaneda, na Argentina, em 29 de dezembro de 2020 — Foto: Natacha Pisarenko/AP
A farmacêutica União Química e o Fundo Russo de Investimento Direto (RDIF) anunciaram, nesta quarta (13), que vão enviar o pedido de uso emergencial da vacina russa Sputnik V contra a Covid-19 ainda nesta semana para a Agência Nacional de Vigilância Sanitária (Anvisa). As informações são do G1.
A Sputnik V é a mesma vacina que começou a ser aplicada na Argentina e em Belarus, e foi a primeira a ser registrada no mundo contra a Covid-19, em agosto.
Para conseguir a autorização, é pré-requisito estar em fase 3 de testes no Brasil. O pedido para estudos em humanos no país foi feito à Anvisa em 29 de dezembro e ainda não foi aprovado. Segundo a empresa, a vacina foi aprovada para uso emergencial em outros países, incluindo “Argentina, Bolívia, Argélia, Sérvia e Palestina”.
O RDIF e a União Química também anunciaram acordo para o envio de 10 milhões de doses da vacina ao Brasil até março, com a primeira entrega prevista para janeiro.
No domingo (8), a farmacêutica informou que começaria a produzir doses da vacina no país “ainda em janeiro”, pela Fábrica Bthek, em Brasília. A empresa prevê o fornecimento de até 8 milhões de doses por mês.
Vacina no Brasil
Quatro vacinas receberam autorização para testes de fase 3 no Brasil desde o início da pandemia. A mais recente a obter foi a Ad26.COV2.S, desenvolvida pela Janssen Pharmaceuticals, do grupo Johnson & Johnson, em agosto de 2020.
Antes, receberam a mesma autorização a vacina de Oxford (inglesa); a Coronavac, da Sinovac (chinesa); e a da BioNTech/Pfizer(alemã/americana).











Deixe um comentário